Demenz gilt noch immer als Schicksal des Alters, als etwas, das irgendwann einfach passiert, unaufhaltsam, genetisch bedingt und ohne es beeinflussen zu können. Diese Sichtweise ist bequem, greift aber viel zu kurz. Sie blendet vollständig aus, was Forschung und klinische Erfahrung seit Jahren zeigen: in den meisten Fällen ist Demenz kein plötzliches Ereignis, sondern das Ergebnis eines jahrelangen, oft jahrzehntelangen Ungleichgewichts im Körper.
Wer Demenz ganzheitlich betrachtet, erkennt sie nicht nur als Erkrankung des Gehirns, sondern als systemisches Geschehen, in dem Entzündung, Stoffwechsel, Darm, Hormone, Nährstoffversorgung, Stress und Lebensweise ineinandergreifen. Genau darin liegt auch eine große Chance, denn Prozesse, die sich langsam entwickeln, lassen sich in ihrer Dynamik oft noch beeinflussen oder zumindest in ihrer Geschwindigkeit verändern.
Demenz ist kein isoliertes Gehirnproblem
Das Gehirn macht nur etwa zwei Prozent unseres Körpergewichts aus und verbraucht dennoch rund zwanzig Prozent der gesamten Energie. Es ist auf eine kontinuierliche Versorgung mit Sauerstoff, Glukose, Fetten, Mikronährstoffen und hormonellen Signalen angewiesen. Gerät dieses fein abgestimmte System aus dem Gleichgewicht, leidet zuerst die geistige Leistungsfähigkeit, oft lange bevor eine formale Diagnose gestellt wird.
Dabei ist es wichtig, normale Schwankungen von krankhaften Veränderungen zu unterscheiden. Viele Menschen erleben Gedächtnislücken, Konzentrationsprobleme oder Wortfindungsphänomene, ohne dass dies etwas mit neurodegenerativen Prozessen zu tun hat. Mehrsprachigkeit, hoher mentaler Anspruch, Schlafmangel, Stress oder hormonelle Verschiebungen können den Zugriff auf gespeicherte Informationen vorübergehend verlangsamen, ohne dass Strukturen verloren gehen. Das Gehirn arbeitet in diesen Momenten nicht schlechter, sondern unter anderen inneren Bedingungen.
Hinzu kommt, dass geistige Leistungsfähigkeit nicht konstant ist, sondern einem inneren Rhythmus folgt. Aufmerksamkeit, Sprachabruf, Arbeitsgedächtnis und Problemlösefähigkeit schwanken im Tagesverlauf deutlich und diese Schwankungen sind genetisch geprägt. Früh-, Normal- und Spättypen haben sehr unterschiedliche Zeitfenster, in denen ihr präfrontaler Kortex, also jene Hirnregion, die für Planung, Sprache und komplexes Denken zuständig ist, optimal arbeitet. Ein chronobiologischer Spättyp kann in den frühen Stunden geistig deutlich eingeschränkt wirken und am Abend oder in der Nacht eine außergewöhnliche Klarheit und geistige Beweglichkeit zeigen.
Gerade bei Menschen, die mehrere Sprachen verwenden, wird dieser Effekt besonders sichtbar. Das Gehirn verwaltet mehrere parallele Sprachsysteme, die im Alltag ständig konkurrieren. In biologischen Tiefphasen wird dieser Zugriff langsamer, Wörter liegen „auf der Zunge“, tauchen aber zuerst in einer anderen Sprache auf oder bleiben kurz blockiert. In den eigenen Hochphasen hingegen funktioniert derselbe Mensch mühelos, präzise und oft sogar besonders kreativ. Diese Phänomene sind Ausdruck eines rhythmischen, hochadaptiven Nervensystems, nicht eines beginnenden geistigen Abbaus.
Relevant werden Veränderungen erst dann, wenn sie neu auftreten, sich verstärken, den Alltag spürbar beeinträchtigen oder unabhängig von Tageszeit, Schlaf und Belastung bestehen bleiben. Erst in diesem Kontext können sie Hinweise auf ein System sein, das zunehmend unter biologischer Überlastung gerät.
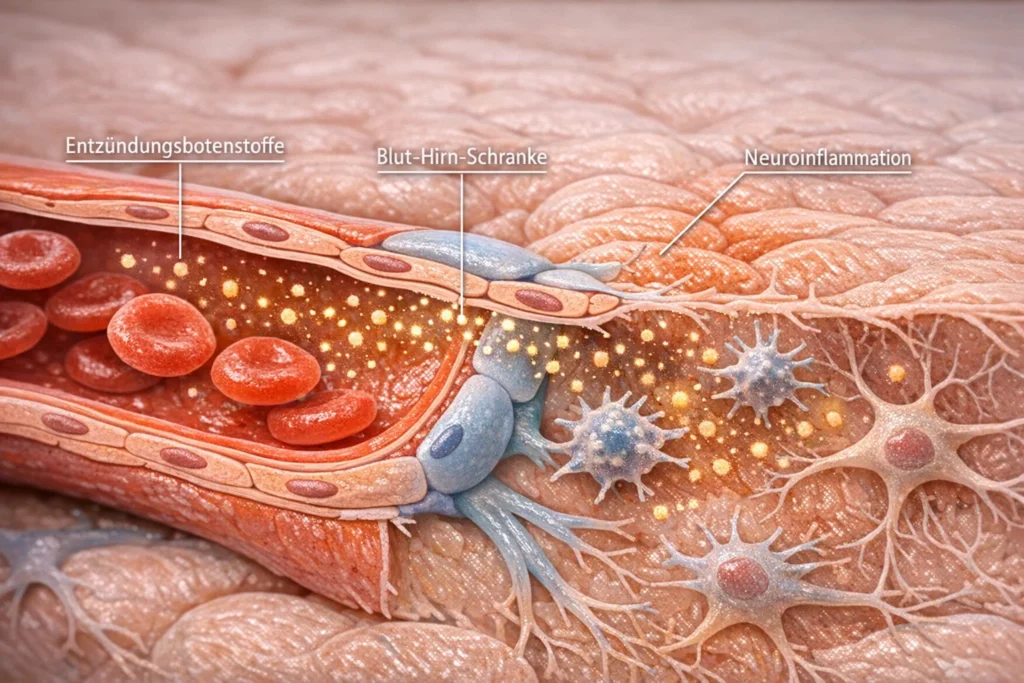
Chronische Entzündung, der stille Brand im Hintergrund
Ein zentraler Treiber dieses Prozesses ist eine chronische, niedriggradige Entzündung. Anders als akute Entzündungen, die mit Schmerz, Fieber oder Schwellung einhergehen, entwickelt sie sich leise im Hintergrund. Sie entsteht, wenn das Immunsystem über lange Zeit immer wieder kleine Reize verarbeiten muss, etwa durch Blutzuckerschwankungen, oxidativen Stress, bakterielle Fragmente aus dem Darm, Schlafmangel oder dauerhafte Aktivierung der Stressachsen. Diese Reize sind für sich genommen nicht dramatisch, in ihrer Summe halten sie das Immunsystem jedoch in einem Zustand ständiger Alarmbereitschaft.
Stark verarbeitete Ernährung, hohe Zuckerlast, Bewegungsmangel, chronischer Stress und eine gestörte Darmflora verstärken diese unterschwellige Aktivierung. Immunzellen beginnen dauerhaft entzündliche Botenstoffe auszuschütten, ohne dass ein klarer Feind vorhanden wäre. So entsteht ein entzündliches Milieu, das sich schleichend im gesamten Körper ausbreitet.
Diese Entzündungsprozesse bleiben nicht auf einzelne Gewebe begrenzt. Über den Blutkreislauf erreichen die Botenstoffe auch das Gehirn. Sie können die Blut Hirn Schranke durchlässiger machen und dort Mikrogliazellen aktivieren, die wiederum neuroinflammatorische Prozesse in Gang setzen. Bei Menschen mit Alzheimer lassen sich solche Veränderungen oft lange vor dem Auftreten klarer Symptome nachweisen.
Insulinresistenz im Gehirn, der metabolische Aspekt der Demenz
Parallel zu den entzündlichen Prozessen spielt der Stoffwechsel eine zentrale Rolle. Immer mehr Forschung deutet darauf hin, dass Alzheimer auch als eine Form von Insulinresistenz im Gehirn verstanden werden kann. Nervenzellen sind auf Glukose als Hauptenergiequelle angewiesen, doch diese Energie steht ihnen nur zur Verfügung, wenn Insulin die Aufnahme in die Zellen ermöglicht. Wird diese Signalwirkung gestört, entsteht ein Mangelzustand, obwohl im Blut genügend Zucker vorhanden ist.
Ein dauerhaft instabiler Blutzucker mit wiederkehrenden Insulinspitzen führt dazu, dass die Insulinrezeptoren im Laufe der Zeit weniger empfindlich werden. Dieser Mechanismus, der im restlichen Körper zur klassischen Insulinresistenz beiträgt, findet auch im Gehirn statt. Gleichzeitig fördern Entzündungsprozesse diese Störung zusätzlich, da entzündliche Botenstoffe direkt in die Insulinsignalketten eingreifen.
Die Folge ist, dass Nervenzellen ihre Energie nicht mehr effizient nutzen können. Das Gehirn gerät in einen Zustand chronischen Energiemangels, der sich zunächst in Konzentrationsschwierigkeiten, geistiger Ermüdung und verminderter geistiger Flexibilität zeigt und später in strukturellem Abbau. In diesem Zusammenhang ist der Begriff Diabetes Typ 3 entstanden, um die enge Verbindung zwischen Stoffwechselstörungen und neurodegenerativen Prozessen zu beschreiben.
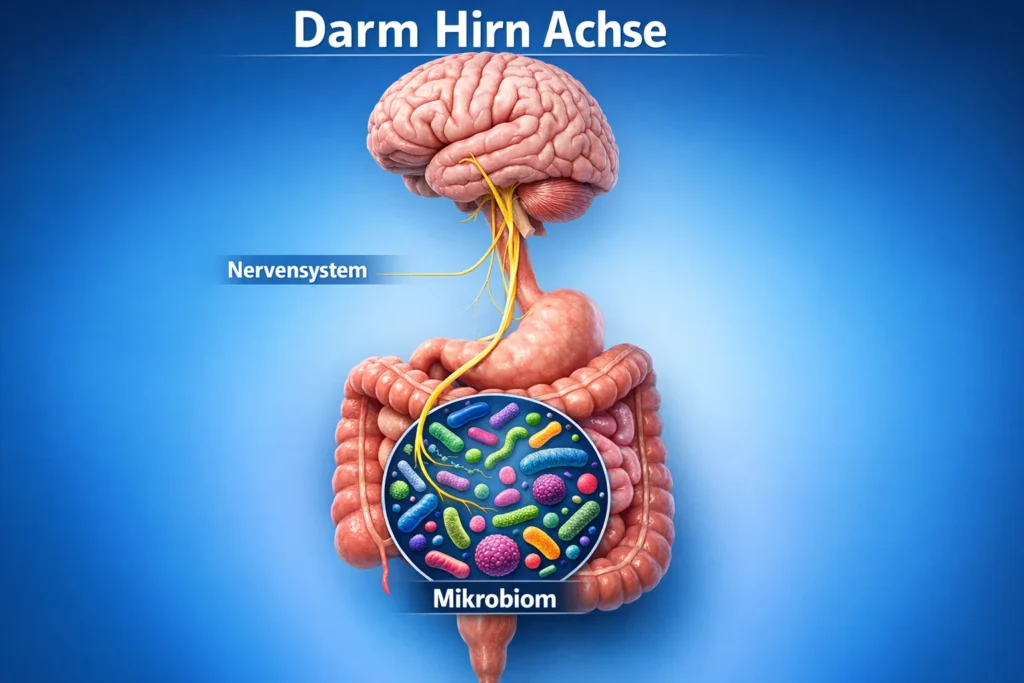
Darm und Mikrobiom, die vergessene Achse
Der Darm bildet eine weitere, oft unterschätzte Schaltzentrale in diesem Geschehen. Über die Darm Hirn Achse steht er in ständigem Austausch mit dem Nervensystem, dem Immunsystem und dem Stoffwechsel. Milliarden von Mikroorganismen produzieren dort fortlaufend Botenstoffe, Stoffwechselprodukte und Neurotransmittervorstufen, die über Nervenbahnen, Blut und Immunwege direkt auf das Gehirn wirken.
Ist das Mikrobiom aus dem Gleichgewicht geraten, etwa durch Ernährung, Antibiotika, chronischen Stress oder Entzündung, verändert sich diese Signalkaskade. Bestimmte Bakterien produzieren weniger entzündungshemmende Metabolite, während andere vermehrt Substanzen freisetzen, die das Immunsystem aktivieren. Gleichzeitig kann die Darmschleimhaut durchlässiger werden, sodass bakterielle Bestandteile in den Blutkreislauf gelangen und systemische Entzündungsreaktionen verstärken.
Diese immunologischen Signale erreichen auch das Gehirn. Sie können die Blut Hirn Schranke beeinflussen, Mikrogliazellen aktivieren und neuroinflammatorische Prozesse verstärken. Gleichzeitig beeinträchtigt eine gestörte Darmfunktion die Aufnahme und Aktivierung vieler Nährstoffe, die für neuronale Energieproduktion, Neurotransmitterbildung und antioxidativen Schutz notwendig sind. So entsteht eine Verbindung zwischen Darm, Entzündung, Stoffwechsel und geistiger Stabilität, die weit über Verdauung hinausgeht.
Nährstoffe als Voraussetzung für geistige Stabilität
Viele Menschen mit geistigem Abbau tragen über Jahre hinweg ein unsichtbares Gepäck aus Mikronährstoffdefiziten mit sich. Die Ursache liegt dabei selten in der Menge der Nahrung, sondern in ihrer Qualität und in der Fähigkeit des Körpers, das Aufgenommene tatsächlich zu nutzen. Eine zunehmend industriell geprägte Ernährung, kombiniert mit einer durch Stress, Entzündung und Darmdysbiose geschwächten Aufnahme, verschiebt das innere Milieu schleichend in einen Zustand chronischer Unterversorgung. Das Gehirn, eines der nährstoffsensibelsten Organe überhaupt, reagiert auf diese Verschiebung besonders früh.
B Vitamine und Folsäure spielen dabei eine zentrale Rolle, weil sie an nahezu allen Prozessen beteiligt sind, die Nervenzellen funktionsfähig halten. Sie steuern die Bildung von Neurotransmittern, den Aufbau der Myelinscheiden, die Methylierung zahlreicher Gene und den Abbau von Homocystein, einer Substanz, deren chronisch erhöhte Spiegel mit einem deutlich höheren Risiko für geistigen Abbau in Verbindung stehen. Fehlen diese Vitamine über längere Zeit, geraten neuronale Reparaturmechanismen, Signalübertragung und Gefäßgesundheit zunehmend unter Druck.
Omega drei Fettsäuren, insbesondere DHA, bilden einen strukturellen Bestandteil der Zellmembranen im Gehirn. Sie beeinflussen die Beweglichkeit der Membranen, die Effizienz der Signalübertragung zwischen Nervenzellen und die Entzündungsbereitschaft des Gewebes. Sinkt ihre Verfügbarkeit, verändert sich die physikalische und biochemische Stabilität der Nervenzellen, was sie anfälliger für Entzündung, oxidativen Stress sowie degenerative Prozesse macht.
Magnesium wirkt im Nervensystem wie ein Puffer. Es reguliert die Erregbarkeit der Nervenzellen, stabilisiert synaptische Funktionen und schützt vor übermäßiger Aktivierung. Chronischer Stress, erhöhte Cortisolspiegel und eine dauerhaft hohe neuronale Anspannung erhöhen den Magnesiumverbrauch erheblich, wodurch ein stiller Mangel entstehen kann, der lange unbemerkt bleibt, das Gehirn jedoch zunehmend vulnerabel macht.
Vitamin D wirkt im Gehirn wie ein regulatorisches Hormon. Es beeinflusst, welche Gene im Gehirn aktiv sind und welche nicht, darunter viele, die Entzündungen, die Signalübertragung zwischen Nervenzellen und die Anpassungsfähigkeit des Gehirns steuern. Wenn die Werte zu niedrig sind, wird das Gehirn anfälliger für Entzündungen und verliert einen Teil seiner eigenen Schutzfunktion, was sich langfristig auf die geistige Stabilität auswirken kann. Hinzu kommt, dass die in vielen europäischen Ländern als ausreichend geltenden Blutwerte vergleichsweise niedrig angesetzt sind. Während in Deutschland oft bereits Spiegel um 20 ng/ml als akzeptabel gelten, bewegen sich funktionelle Zielbereiche in anderen Ländern und in der präventiven Medizin eher im Bereich von 40 bis 60 ng/ml. Dadurch entsteht ein breiter Graubereich, in dem Menschen formal als versorgt gelten, biologisch jedoch bereits in einer Unterversorgung leben, die sich langfristig auf Gehirn, Immunsystem und Entzündungsregulation auswirken kann. Besonders eindrücklich zeigt sich diese Priorisierung in der Stillzeit, denn der Vitamin D Gehalt der Muttermilch hängt direkt vom Vitamin D Status der Mutter ab. Erst bei gut gefüllten Speichern steigt die Abgabe an den Säugling deutlich an, ein Hinweis darauf, dass der Körper Vitamin D zunächst für die eigene Stabilität zurückhält und es erst bei ausreichender Versorgung großzügig weitergibt.
Zink ist eng mit Gedächtnisprozessen, synaptischer Kommunikation und der Immunbalance im Nervensystem verknüpft. Sowohl Defizite als auch Überversorgungen können die neuronale Funktion beeinträchtigen, was zeigt, wie fein austariert diese Spurenelemente im Gehirn wirken.
Auch Eisen bewegt sich in einem engen biologischen Korridor. Ein Mangel reduziert die Sauerstoffversorgung des Gehirns und damit die mitochondriale Energieproduktion, ein Überschuss fördert oxidative Schäden und Entzündungsreaktionen. Beides kann langfristig die geistige Leistungsfähigkeit untergraben.
In der Summe zeigt sich, dass Mikronährstoffe keine isolierten Stellschrauben sind, sondern Teil eines hochsensiblen Systems, in dem Energieproduktion, Neurotransmission, Immunregulation und strukturelle Integrität ineinandergreifen. Wenn dieses System über längere Zeit nicht richtig versorgt wird und seine innere Balance verliert, nimmt auch die Widerstandskraft des Gehirns ab, die es eigentlich vor dem Abbau schützt.
Für Leserinnen und Leser, die diesen Zusammenhang weiter vertiefen möchten, etwa im Hinblick auf Zucker, Gluten und Alkohol als schleichende Störfaktoren von Darm, Entzündung und Nährstoffverwertung, bietet mein Artikel „Ein bisschen davon macht doch nichts aus“ eine passende Erweiterung dieses Gedankens.
Mitochondrien und der schleichende Energieverlust
Auf zellulärer Ebene spielen die Mitochondrien eine entscheidende Rolle. Sie sind die Kraftwerke der Zellen und versorgen insbesondere Nervenzellen mit der Energie, die sie für Signalübertragung, Reparaturprozesse und Plastizität benötigen. Das Gehirn gehört zu den energiehungrigsten Organen überhaupt, weshalb mitochondriale Störungen hier besonders früh spürbar werden.
Oxidativer Stress, chronische Entzündung, Nährstoffmängel und Umweltgifte greifen diese empfindlichen Strukturen über Jahre hinweg an. Freie Radikale, die unter Stress, durch Entzündungen oder durch Schadstoffe vermehrt entstehen, beschädigen die Membranen und die DNA der Mitochondrien. Gleichzeitig fehlen bei mangelhafter Ernährung oder gestörter Darmaufnahme jene Vitamine, Mineralstoffe und Fettsäuren, die für ihre Funktion notwendig wären. Auch dauerhaft erhöhte Blutzucker und Insulinspiegel belasten die Mitochondrien, weil sie die Energieverarbeitung ineffizient machen und zusätzliche oxidative Prozesse auslösen.
Die Folge ist ein schleichender Verlust an zellulärer Energie. Nervenzellen geraten zunehmend in einen Mangelzustand, in dem sie ihre komplexen Aufgaben nicht mehr aufrechterhalten können. Dieser Energiemangel zeigt sich zunächst als geistige Müdigkeit, als nachlassende Konzentration und geringere Belastbarkeit und geht im Laufe der Zeit in strukturellen Abbau über.
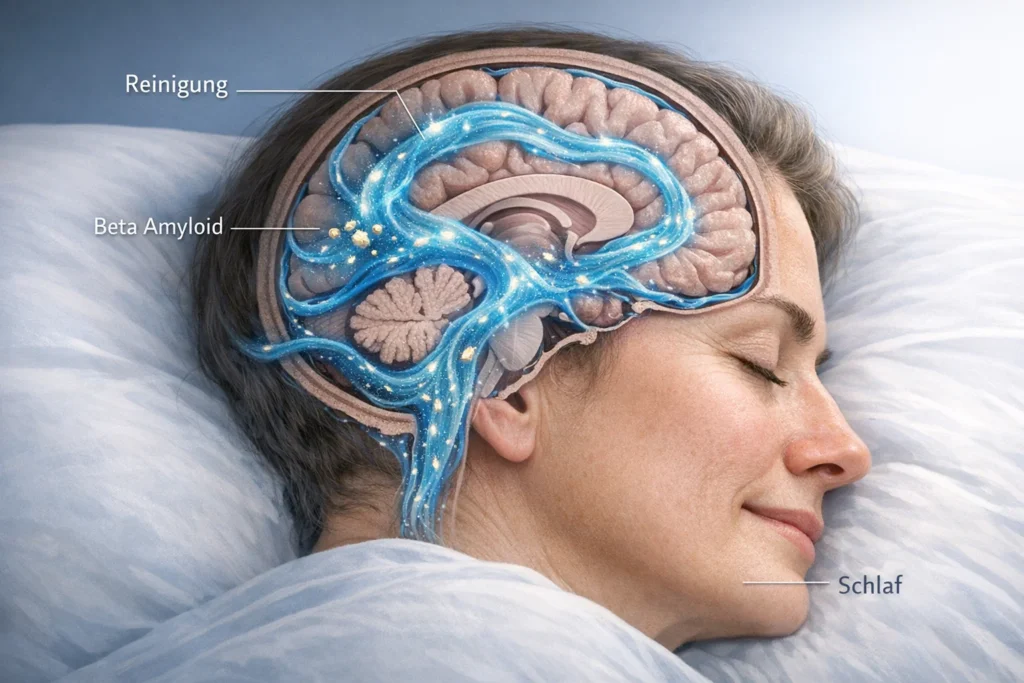
Schlaf, Stress, Cortisol und neuronische Erschöpfung
Chronischer Stress greift tief in die Steuerung des Gehirns ein. Wenn der Körper über lange Zeit im Alarmmodus bleibt, wird vermehrt Cortisol ausgeschüttet, ein Hormon, das eigentlich kurzfristig helfen soll, mit Gefahr umzugehen. Bleibt dieser Zustand jedoch bestehen, beginnt er, genau jene Strukturen zu belasten, die für Lernen, Gedächtnis und emotionale Stabilität wichtig sind. Im Hippocampus, einem zentralen Bereich für Erinnerung und Orientierung, wird die Neubildung von Nervenzellen gehemmt, während entzündliche Prozesse zunehmen und der Zuckerstoffwechsel aus dem Gleichgewicht gerät. Das Gehirn bleibt in einer Art Daueranspannung gefangen, in der Schutzreaktionen dominieren und regenerative Prozesse immer schwerer greifen.
Viele Menschen erleben diesen Zustand als innere Unruhe, Reizbarkeit, Gedankenkreisen oder das Gefühl, nie wirklich zur Ruhe zu kommen. Der Körper versucht ständig, sich anzupassen, doch ohne ausreichend Erholung wird diese Anpassung zur Erschöpfung. Besonders belastend ist, dass dieser biologische Stress in unserer Kultur oft als individuelles Versagen wahrgenommen wird, als mangelnde Belastbarkeit oder fehlende Selbstdisziplin, obwohl es sich in Wirklichkeit um eine messbare Verschiebung im Nervensystem handelt.
Der Schlaf ist in diesem Zusammenhang einer der wichtigsten Gegenpole. In den tiefen Schlafphasen fährt das Gehirn seine Alarmprogramme herunter und aktiviert seine Reparaturmechanismen. Nervenzellen werden stabilisiert, Verbindungen neu geordnet, Stoffwechselabfälle abtransportiert und Stresshormone reguliert. Schon wenige Nächte mit schlechtem oder unterbrochenem Schlaf reichen aus, um Konzentration, Gedächtnis und emotionale Stabilität spürbar zu beeinträchtigen. Wenn dieser Zustand über Monate oder Jahre anhält, verstärkt sich der Effekt und trägt dazu bei, dass das Gehirn seine Widerstandskraft gegenüber Entzündung, Stoffwechselstress und Alterungsprozessen verliert.
Warum Demenz gesellschaftlich so spät gesehen wird
Auf gesellschaftlicher Ebene kommt hinzu, dass Demenz Angst auslöst. Sie berührt Fragen wie Kontrolle, Abhängigkeit oder auch die nach Identität. Diese Angst führt fatalerweise oft zu einem inneren Wegsehen sowohl bei Betroffenen, als auch im Umfeld und in institutionellen Strukturen.
Frühe Anzeichen von Vergesslichkeit, Orientierungsschwierigkeiten oder emotionale Veränderungen werden deshalb häufig relativiert oder als Alterserscheinung, als Stress oder als vorübergehende Phase erklärt. Dahinter liegt oft der Wunsch, eine mögliche Diagnose nicht denken zu müssen. In einer Kultur, die Funktionieren und Autonomie hoch bewertet, wird geistiger Abbbau eben als Bedrohung erlebt.
Hinzu kommt, dass das Gesundheitssystem vor allem auf akute Ereignisse ausgerichtet ist. Demenz beginnt jedoch leise über lange Zeiträume hinweg. Zwischen unauffällig und klinisch eindeutig liegt eine lange Phase, in der biologische Prozesse bereits kippen, ohne klar benannt zu werden. In dieser Zeit wäre noch vieles möglich, doch sie wird oft übersehen.
Frühe Aufmerksamkeit hätte hier eine andere Qualität. Sie würde nicht stigmatisieren, sondern Ressourcen sichtbar machen, Entlastung ermöglichen und das innere System stabilisieren, solange es noch beweglich ist. Je früher wir hinschauen, desto größer bleibt der Handlungsspielraum, dem Körper helfen zu können, sich selbst wieder zu regulieren!
Was frühe Gegenregulation bedeutet
Wenn Demenz aus einem langen biologischen Ungleichgewicht entsteht, dann liegt in dieser Langsamkeit auch ihre besondere Bedeutung. Der Körper verliert seine geistige Stabilität nicht von einem Moment auf den anderen, sondern in kleinen Verschiebungen über Jahre hinweg. Und genau in diesen Verschiebungen lässt sich Richtung geben.
Frühe Gegenregulation bedeutet, das innere Milieu zu verändern, in dem das Gehirn altert. Es geht um die Bedingungen, unter denen Nervenzellen dauerhaft im Überlebensmodus stehen oder wieder Zugang zu Reparatur, Plastizität und Regeneration finden.
Das beginnt bei den zwei grundlegenden biologischen Rhythmen Schlaf und Ernährung.
Im Schlaf regeneriert sich das Gehirn, baut Abfallstoffe ab, stabilisiert neuronale Netzwerke und reguliert Stresshormone. Während Während tiefer Schlafphasen wird das glymphatische System aktiv, ein Reinigungssystem des Gehirns, das Stoffwechselabfälle wie Beta Amyloid, ein Eiweiß, das sich bei Alzheimer in schädlichen Ablagerungen ansammelt, abtransportiert. Wird dieser Prozess über Jahre hinweg durch Schlafmangel, Schichtarbeit oder innere Unruhe gestört, bleiben diese Substanzen im Gewebe zurück und fördern neurodegenerative Veränderungen.
Auch die Ernährung wirkt auf diese Prozesse ein, weil sie fortlaufend biochemische Signale an den Körper sendet. Jede Mahlzeit beeinflusst Entzündung, Blutzucker, Insulinantwort und das Mikrobiom. Eine Ernährung, die über lange Zeit reich an Zucker, stark verarbeiteten Fetten und nährstoffarmen Produkten ist, verschiebt dieses Milieu in Richtung Entzündung und metabolische Instabilität. Eine nährstoffdichte, pflanzenbetonte, ballaststoffreiche und eiweißhaltige Kost ohne Industriezucker jeglicher Art kann dieses Gleichgewicht wieder in eine andere Richtung bewegen.
Für das Gehirn ist dabei besonders die Stabilität des Blutzuckers entscheidend. Es ist auf eine gleichmäßige Energieversorgung angewiesen. Ständige Schwankungen erzeugen Stress im Nervensystem, verstärken Entzündungsprozesse und begünstigen langfristig Insulinresistenz auch im Gehirn. Mahlzeiten, die komplexe Kohlenhydrate, pflanzliche Fette, Proteine und Ballaststoffe verbinden, wirken hier ausgleichend. All das bietet eine pflanzenbetonte Ernährungsweise, vorzugsweise biologischer Herkunft, da auch Pestizide da auch Pestizide als Umweltgifte den Körper und insbesondere den Darm belasten.
Über den Darm wirkt Ernährung zusätzlich auf die Neuroinflammation, also auf entzündliche Prozesse im Gehirn. Ballaststoffe, Polyphenole und fermentierbare Pflanzenstoffe, alles in der pflanzenbetonten Ernährung reichlich vorkommende Stoffe, nähren genau die Bakterien im Darm, die kurzkettige Fettsäuren bilden und die Darm Hirn Achse stabilisieren. Auf diesem Weg lässt sich die Entzündungsbereitschaft im Gehirn zum Positiven beeinflussen, lange bevor strukturelle Schäden entstehen.
Auch die Versorgung mit Mikronährstoffen gehört zu dieser frühen Gegenregulation. B Vitamine, Omega drei Fettsäuren, Magnesium, Vitamin D, Zink und eine ausgeglichene Eisenversorgung bilden die Grundlage dafür, dass Nervenzellen stabil bleiben, die Signalstoffe im Gehirn im Gleichgewicht sind und die Mitochondrien, also die Kraftwerke der Zellen, ausreichend Energie bereitstellen können. Defizite entstehen langsam und bleiben oft lange unbemerkt, können jedoch über Jahre hinweg die Widerstandskraft des Gehirns schwächen.
Stressregulation
Neben Schlaf und Ernährung prägt das Nervensystem entscheidend, in welchem inneren Klima das Gehirn lebt. Wenn der Körper über lange Zeit im Alarmzustand bleibt, weil Stress, Überforderung oder innere Unsicherheit nicht abklingen, wird das gesamte System auf Überleben statt auf Regeneration ausgerichtet. Entzündungsprozesse nehmen zu, die Durchblutung verändert sich, der Schlaf wird flacher und die Fähigkeit, neue neuronale Verbindungen zu bilden, nimmt ab. Das Gehirn arbeitet dann nicht mehr aus einem Zustand von Stabilität heraus, sondern aus permanenter Anpassung.
Rhythmus, Atmung, Bewegung, soziale Sicherheit und bewusste Pausen wirken in diesem Zusammenhang wie biologische Gegengewichte. Sie signalisieren dem Nervensystem, dass keine akute Gefahr besteht, und ermöglichen es, aus dem Alarmmodus in einen Zustand zu wechseln, in dem Reparatur, Lernen und Regeneration wieder greifen können. Diese scheinbar einfachen Faktoren entscheiden darüber, ob Entzündung gedämpft oder weiter angeheizt wird, ob Energie aufgebaut oder verbraucht wird.
All diese Ebenen greifen ineinander. Sie verändern nicht nur einzelne Werte, sondern das gesamte Milieu, in dem das Gehirn altert. Genau hier liegt die eigentliche Prävention, in der bewussten Gestaltung jener Bedingungen, unter denen geistige Stabilität überhaupt entstehen und erhalten bleiben kann.
Demenz ist kein plötzliches Schicksal
Demenz ist selten ein plötzliches Schicksal. Sie ist meist das Ergebnis einer langen Geschichte biologischer Überlastung, in der Entzündung, Stoffwechsel, Stress, Schlafmangel, Nährstoffdefizite und soziale Belastungen über Jahre hinweg auf dasselbe System einwirken. Wer sie ganzheitlich betrachtet, erkennt darin neben den Risiken auch jene Räume, in denen Einfluss möglich bleibt, lange bevor eine Diagnose unausweichlich erscheint.
Nicht alles lässt sich verhindern. Gene, Lebensgeschichte, Umweltbelastungen und Alter prägen den Weg eines Menschen, aber gleichzeitig lässt sich vieles beeinflussen oder verlangsamen, wenn Gehirn, Körper und Lebenskontext als zusammenhängendes System verstanden werden. Ein Gehirn altert nicht für sich! Es altert in einem Körper, in einem Nervensystem, in einem Alltag, in Beziehungen, in Rhythmen, in Ernährungsgewohnheiten und in einer inneren wie äußeren Umwelt als Gesamtheit.
Hier setzt auch die Epigenetik an. Sie beschreibt jene biologischen Mechanismen, über die Umwelt, Ernährung, Stress, Schlaf und emotionale Erfahrungen steuern, welche Gene in einer Zelle aktiv sind und welche stumm bleiben. Die Gene selbst verändern sich dabei nicht, aber ihr Verhalten, also welche Informationen sie weitergeben, reagiert fortlaufend auf das innere und äußere Milieu. Auf diese Weise wird verständlich, warum Lebensstil, Belastungen und Fürsorge tief in die biologischen Prozesse eingreifen, die langfristig über Gesundheit oder Krankheit mitentscheiden.
Ganzheitliche Gesundheit bedeutet, diese Zusammenhänge ernst zu nehmen und Menschen darin zu unterstützen, wieder Einfluss auf ihr inneres Milieu zu erhalten. Verständnis sowie, Wahrnehmung, aber auch bewusste Gestaltung dessen, was gestaltbar ist, bilden dabei die Grundlage.
So wird der Blick auf Demenz zu einem Blick auf einen Prozess, der, wie alle biologischen Prozesse, in Beziehung zu den Bedingungen steht, unter denen er entsteht.
Du findest meine Beiträge informativ und möchtest keinen verpassen? Dann schließe dich meinen Abonnenten an und bleibe über den Newletter auf dem Laufenden mit allem, was du wissen musst.
Quellen:
- Schlaf, glymphatisches System, Abtransport von Abfallstoffen wie Beta-Amyloid
Xie L. et al. (2013). Sleep drives metabolite clearance from the adult brain. Science.
https://www.science.org/doi/10.1126/science.1241224
Kurzinhalt: Tierexperimentelle Daten zeigen, dass der Interstitialraum im Schlaf zunimmt und der Abtransport von Metaboliten, darunter Beta-Amyloid, deutlich effizienter abläuft als im Wachzustand. - Schlafmangel und Beta-Amyloid im Menschen
Shokri-Kojori E. et al. (2018). β-Amyloid accumulation in the human brain after one night of sleep deprivation. PNAS.
https://www.pnas.org/doi/10.1073/pnas.1721694115
Kurzinhalt: PET-Daten deuten darauf hin, dass eine Nacht Schlafentzug mit messbar erhöhter Beta-Amyloid-Last in bestimmten Hirnregionen assoziiert sein kann. - Lifestyle wirkt, wenn man früh ansetzt, multidomain Prävention (Ernährung, Bewegung, kognitives Training, vaskuläre Risiken)
Ngandu T. et al. (2015). A 2 year multidomain intervention… (FINGER trial). The Lancet.
https://pubmed.ncbi.nlm.nih.gov/25771249/
Kurzinhalt: Randomisierte Studie bei Risikopersonen, eine strukturierte Kombination aus Lebensstilmaßnahmen konnte kognitive Funktionen im Vergleich zur Kontrolle verbessern bzw. stabilisieren. - Insulinresistenz im Gehirn, “Type 3 diabetes” als Konzept
de la Monte S.M. (2008). Alzheimer’s disease is type 3 diabetes, evidence reviewed. J Diabetes Sci Technol.
https://pmc.ncbi.nlm.nih.gov/articles/PMC2769828/
Kurzinhalt: Review, der zusammenfasst, dass Störungen der Insulin, IGF-Signalwege im Gehirn frühe und progressive Merkmale bei Alzheimer sein können, inklusive mechanistischer Tiermodelle und Überschneidungen mit metabolischen Pathologien. - Entzündung und Alzheimer, Neuroinflammation als zentraler Prozess
Heneka M.T. et al. (2015). Neuroinflammation in Alzheimer’s disease. The Lancet Neurology.
https://pubmed.ncbi.nlm.nih.gov/25792098/
Kurzinhalt: Überblick über Mikroglia, Astroglia und angeborene Immunantworten im Gehirn, mit dem Kernpunkt, dass entzündliche Mechanismen in Pathogenese und Progression eine relevante Rolle spielen. - Homocystein als Risikofaktor, B-Vitamine als Ansatz zur Modulation
Smith A.D. et al. (2018). Homocysteine and Dementia, An International Consensus Statement.
https://pubmed.ncbi.nlm.nih.gov/29480200/
Kurzinhalt: Konsensusübersicht, die Homocystein als modifizierbaren Risikofaktor beschreibt und Interventionen mit B-Vitaminen im Kontext von Atrophierate und kognitivem Verlauf diskutiert, mit klarer Einordnung der Evidenzlage. - Homocystein, Dosis-Wirkungs-Zusammenhang und Demenzrisiko
Zhou F. et al. (2019). Dose-response meta-analysis… blood homocysteine and Alzheimer-type dementia risk.
https://pubmed.ncbi.nlm.nih.gov/30826501/
Kurzinhalt: Meta-Analyse prospektiver Daten, höhere Homocysteinspiegel sind dosisabhängig mit höherem Alzheimer-Demenzen-Risiko assoziiert. - Ernährungsmuster, MIND-Diet und Alzheimer-Inzidenz
Morris M.C. et al. (2015). MIND diet associated with reduced incidence of Alzheimer’s disease.
https://pubmed.ncbi.nlm.nih.gov/25681666/
Kurzinhalt: Kohortenbasierte Assoziationen, höhere Adhärenz zur MIND-Ernährung korreliert mit niedrigerer Alzheimer-Inzidenz, auch moderate Adhärenz zeigte Effekte. - MIND-Diet und Demenzrisiko in größerer Population
Chen H. et al. (2023). Association of the MIND Diet With the Risk of Dementia. JAMA Psychiatry.
https://jamanetwork.com/journals/jamapsychiatry/fullarticle/2804268
Kurzinhalt: Beobachtungsdaten, MIND-Adhärenz ist mit niedrigerem Risiko für incident dementia assoziiert, mit dem üblichen Hinweis, dass es Assoziationen sind, keine Kausalbeweise. - Vitamin D und Demenzrisiko, Meta-Analyse
Kalra A. et al. (2020). Association of Vitamin D Levels with incident all-cause dementia and Alzheimer’s disease, a meta-analysis.
https://www.sciencedirect.com/science/article/pii/S2274580724004618
Kurzinhalt: Meta-Analyse prospektiver Studien, niedrige Vitamin-D-Spiegel sind mit höherem Risiko für Demenz und Alzheimer assoziiert, Effektgrößen variieren je nach Cut-offs und Studiendesign. - Mikrobiom und Alzheimer-Spektrum, systematische Übersichtsarbeit und Meta-Analyse
Hung C.C. et al. (2022). Gut microbiota in patients with Alzheimer’s disease spectrum, systematic review and meta-analysis.
https://pmc.ncbi.nlm.nih.gov/articles/PMC8791218/
Kurzinhalt: Zusammenfassung von Studien, die wiederkehrende Unterschiede in Zusammensetzung und Diversität der Darmmikrobiota im Alzheimer-Spektrum gegenüber Kontrollen berichten, inklusive Einordnung der Limitationen. - Bewegung als modifizierbarer Risikofaktor, Meta-Analyse prospektiver Kohorten
Zhang X. et al. (2023). Effect of physical activity on risk of Alzheimer’s disease, a meta-analysis of prospective cohort studies.
https://pubmed.ncbi.nlm.nih.gov/37979700/
Kurzinhalt: Höhere körperliche Aktivität ist in prospektiven Kohorten konsistent mit geringerem Alzheimer-Risiko assoziiert, trotz unvermeidlicher Confounding-Problematik in Observationsdaten.